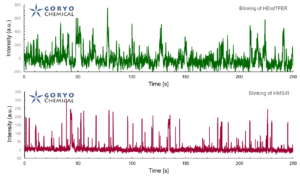
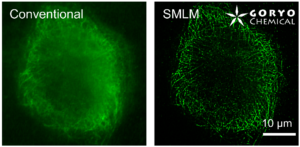
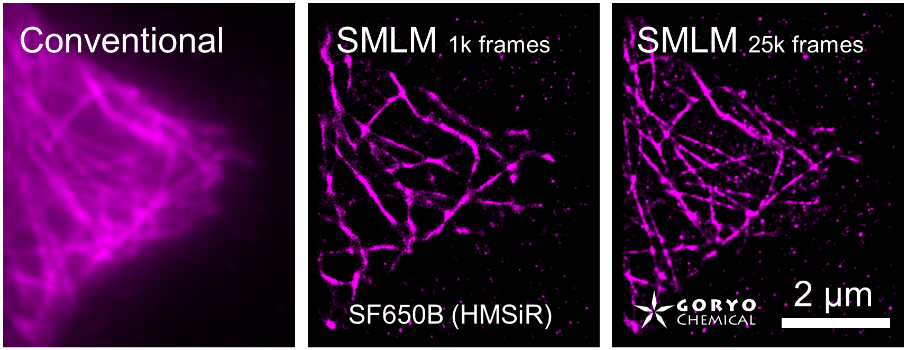
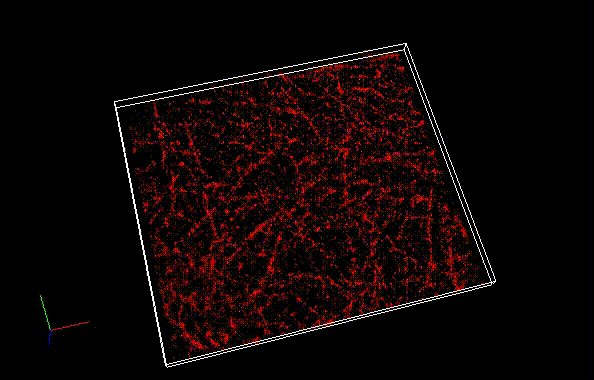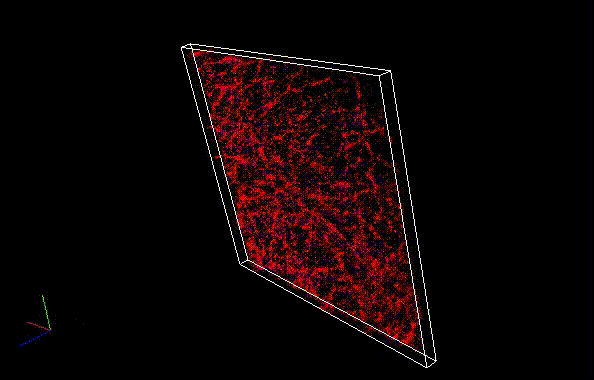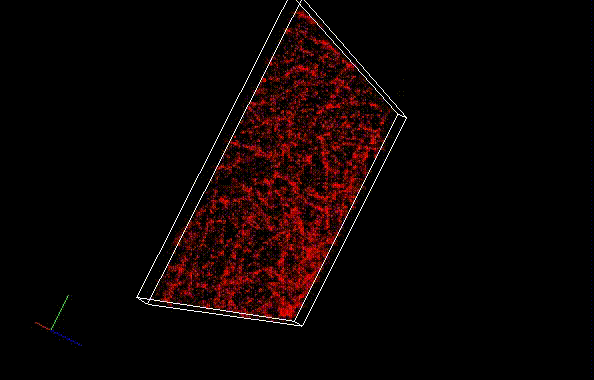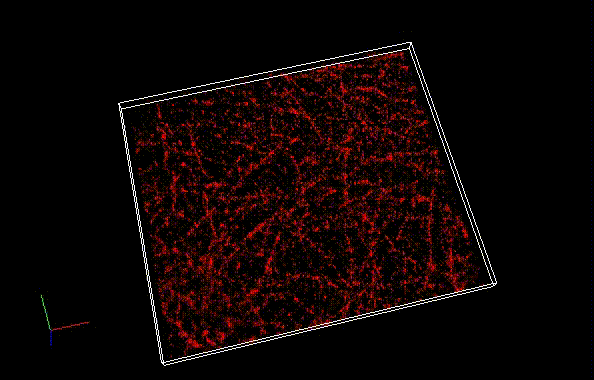
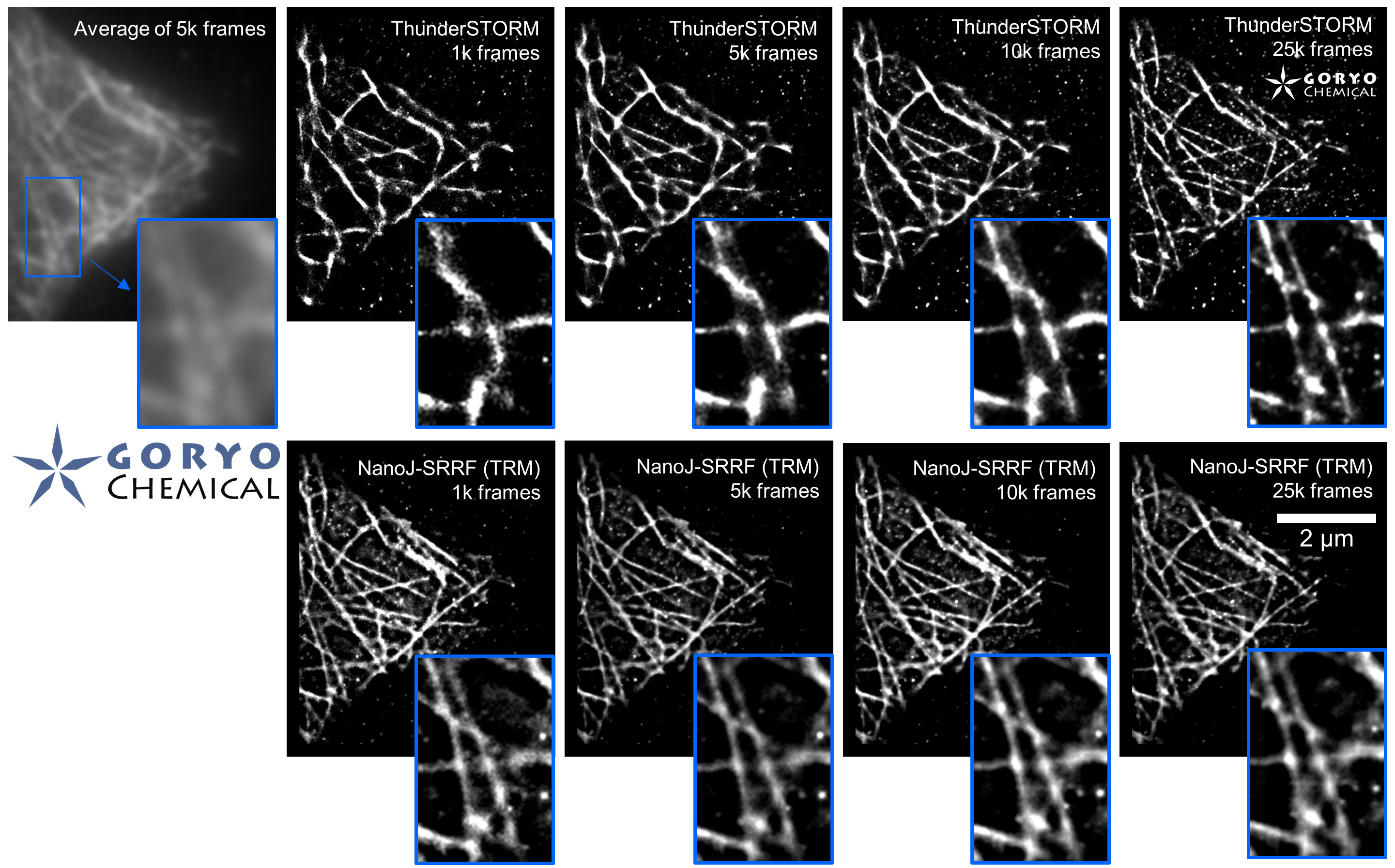
一般的な光学顕微鏡(蛍光顕微鏡)の分解能は波長の約半分(200-400 nm)が理論的な限界です。この限界を超える手法として、「超解像蛍光顕微鏡法」がいくつも開発されてきています。その一つとして、1分子局在化法 (single molecule localization microscopy, SMLM) が広く使われています。SaraFluor B シリーズはこの SMLM 専用に開発された、生理的条件下で自発的点滅を示す蛍光色素です。
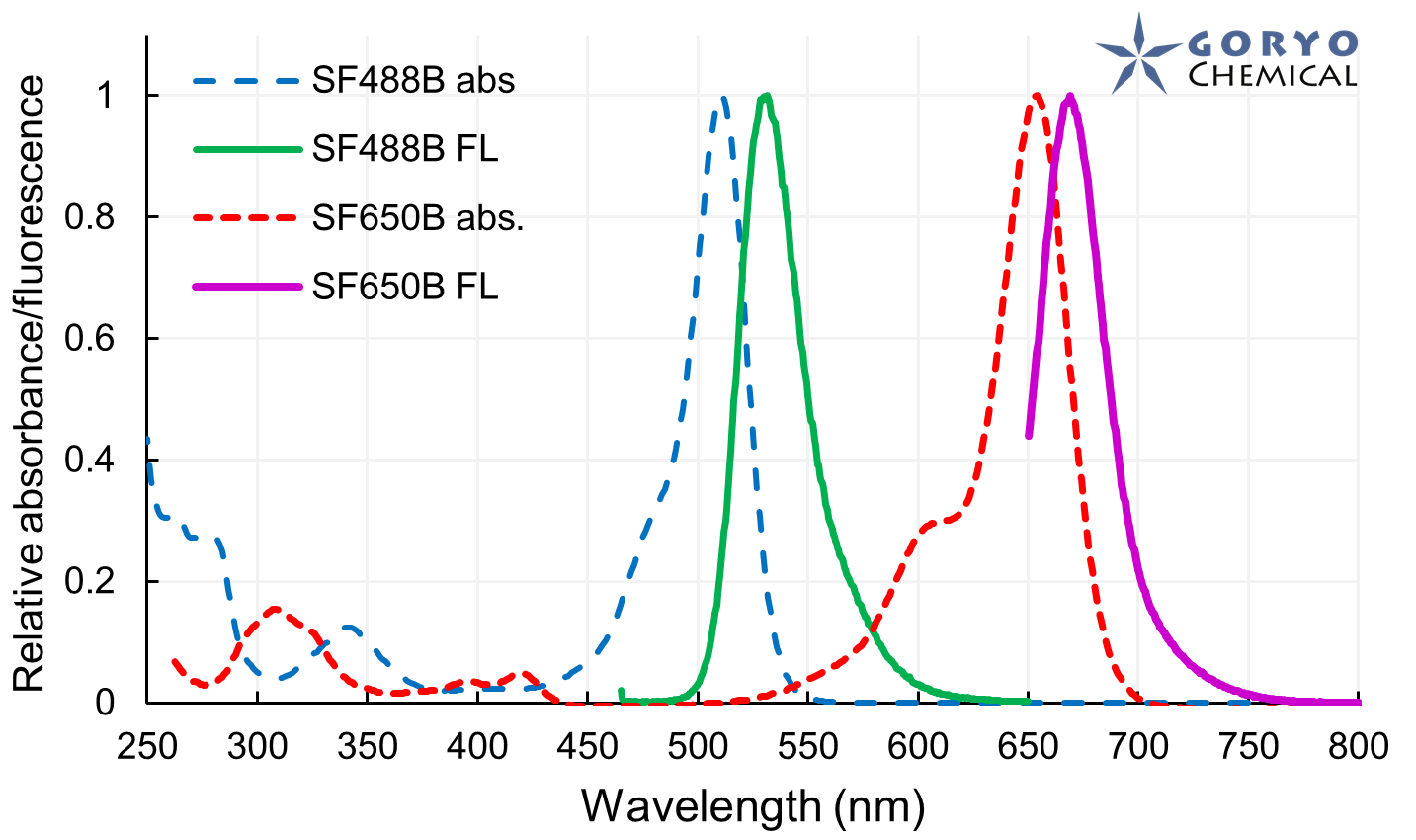
SaraFluor 488B (SF488B, HEtetTFER) は青色レーザー励起によって緑の蛍光を示す色素です。SaraFluor 650B** (SF650B, HMSiR) は赤色レーザー励起によって深赤色の蛍光を示します。抗体など目的のタンパク質やその他の高分子を NHS またはマレイミド基を介して標識することができます。
* SaraFluor はアイヌ語で「見えるようになる」「明るく開けた葦原」などの意味の sara という言葉に由来する造語です。自発的点滅を示す色素は、SaraFluor シリーズの中でも B をつけて区別されています。
** これらの製品はかつて HMSiR-NHS または HMSiR-maleimide という製品名で販売してきたものと同一です。









 メールでのお問い合わせ
メールでのお問い合わせ
