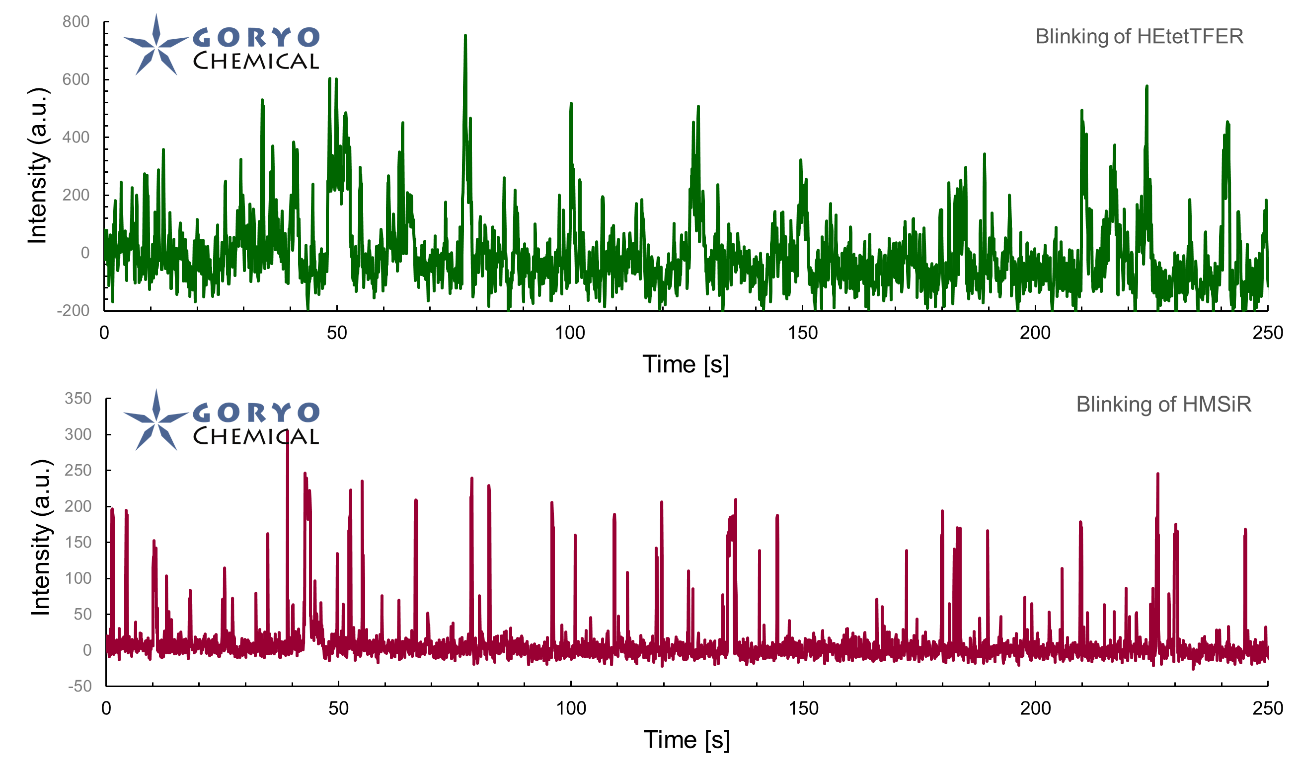
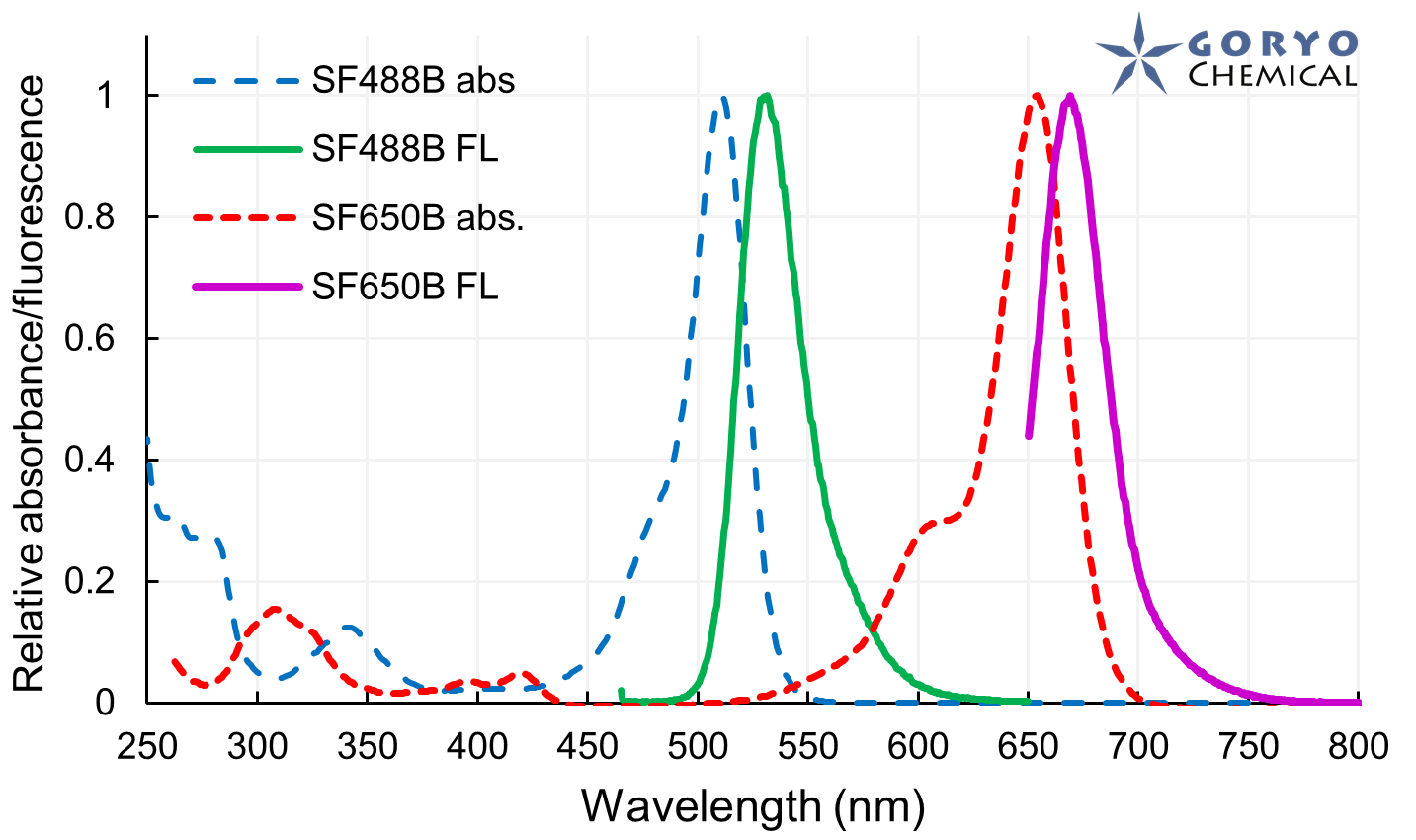
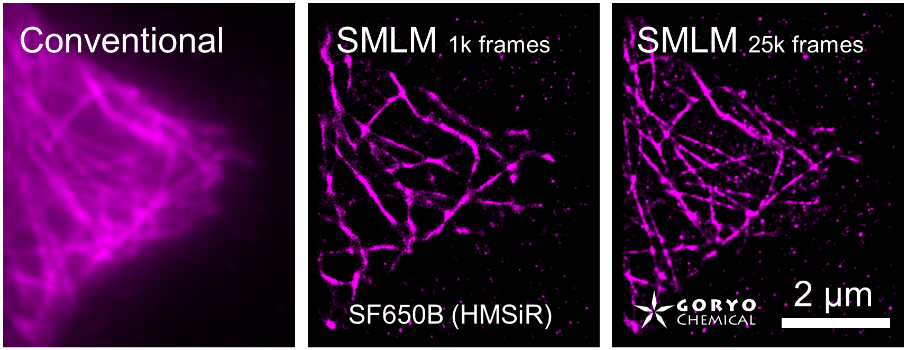
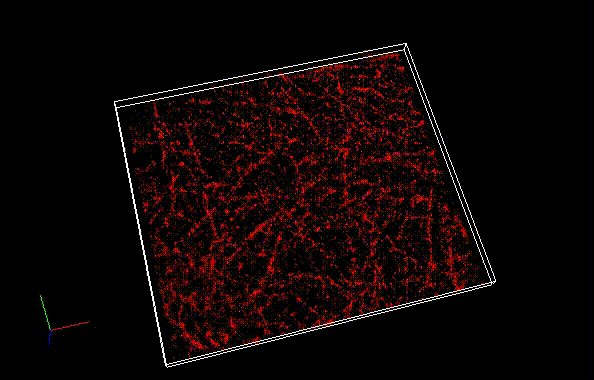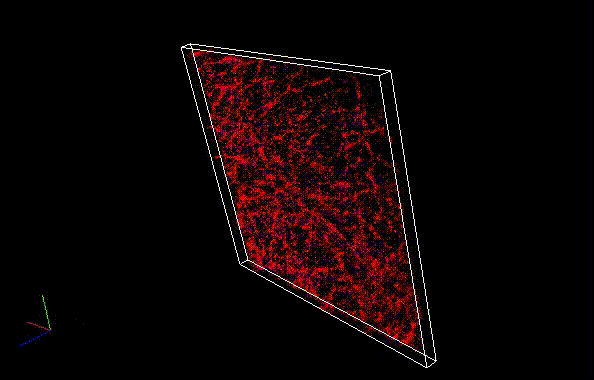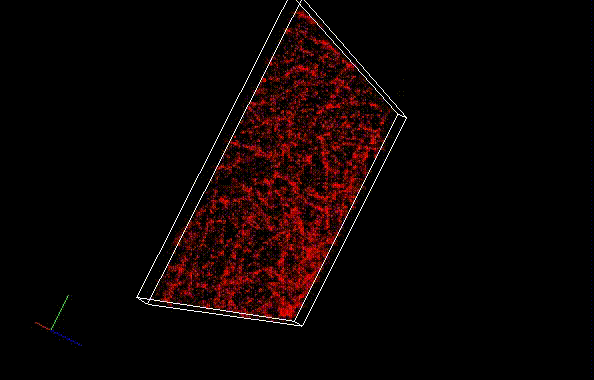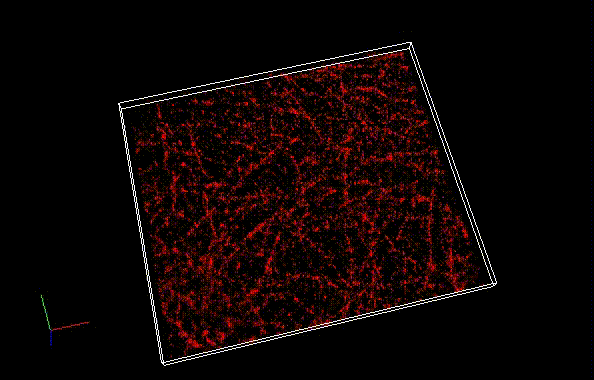
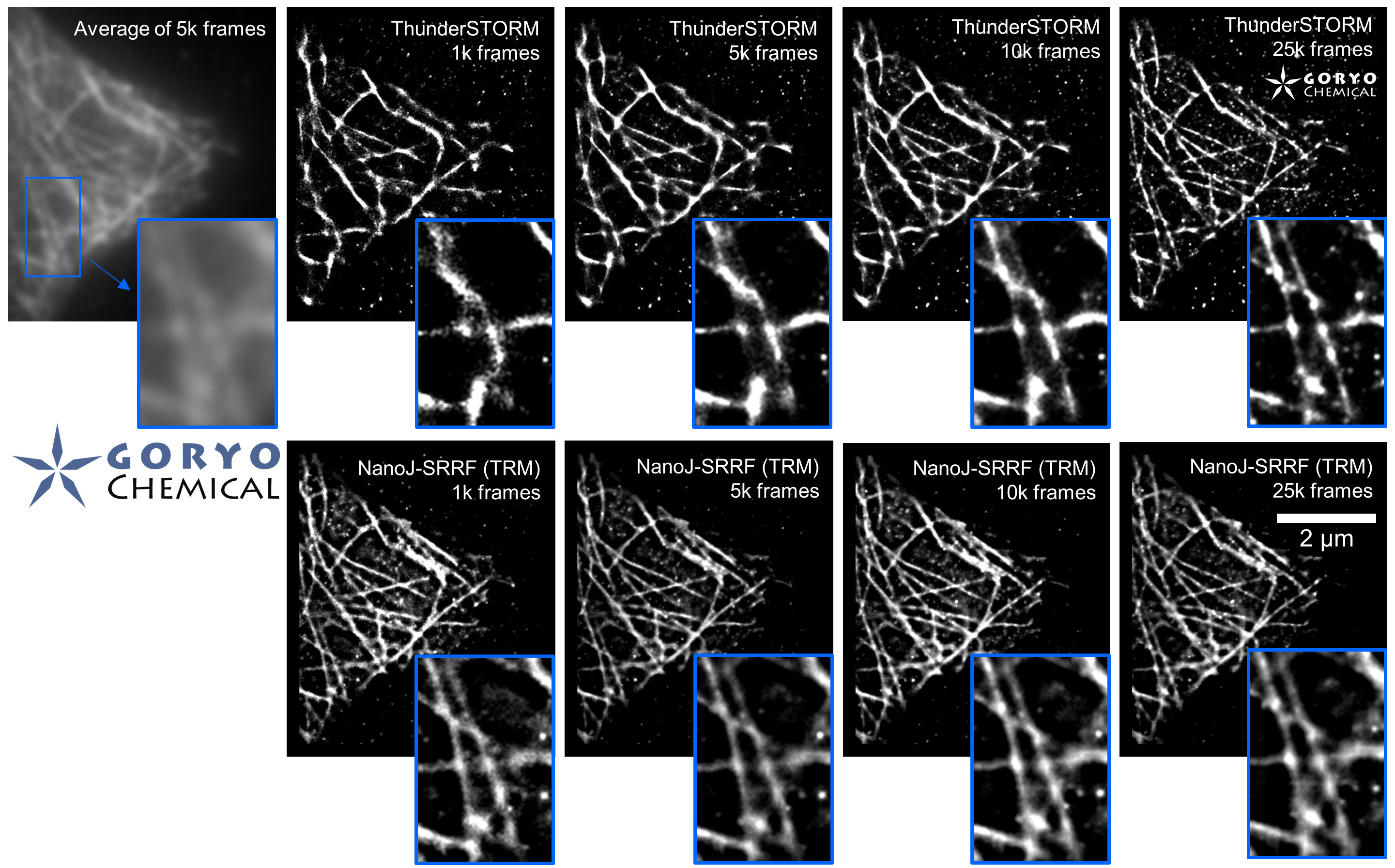
蛍光顕微鏡によるイメージングの分解能は、光の波長の半分程度 (200-400 nm) が理論的な限界とされています。この制約を超える「超解像蛍光顕微鏡法」(superresolution fluorescence microscopy) と呼ばれるイメージング手法の1つとして、1分子局在化法 (single molecule localization microscopy, SMLM) が広く使われています。この SMLM 専用に開発されたSaraFluor B シリーズは生理的条件下で自発的な明滅を行う蛍光色素です。 STORM や PALM といった SMLM 用の顕微鏡システムを用い、蛍光色素を明滅させるためのレーザー照射や還元剤添加を行うことなく簡単に超解像画像を得ることができます。
本製品は免疫蛍光染色用の2次抗体です。
*SaraFluor はアイヌ語で「見えるようになる」「明るく開けた葦原」などの意味の sara という言葉に由来する造語です。自発的明滅を行う SaraFluor 色素には blinking の頭文字の B を付しています。
**各製品はそれぞれ HMSiR 標識 Goat IgG (whole) anti-mouse/rat/rabbit IgG H&L として販売してきたものと同一です。
型番 A202-01 製品名 SaraFluor™650B goat anti-mouse IgG、
型番 A204-01 製品名 SaraFluor™650B goat anti-rabbit IgG は 2025 年 1 月 23 日より販売を中止中です。
型番 A203-01 製品名 SaraFluor™650B goat anti-rat IgG は 2025 年8 月 2日より販売を中止中です。
販売再開に関しては、時期が決まり次第お知らせいたします。
ご不便をおかけいたしますが、何卒ご理解賜りますようお願い申し上げます。








 メールでのお問い合わせ
メールでのお問い合わせ
