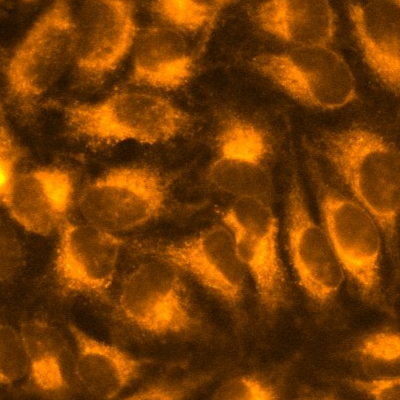
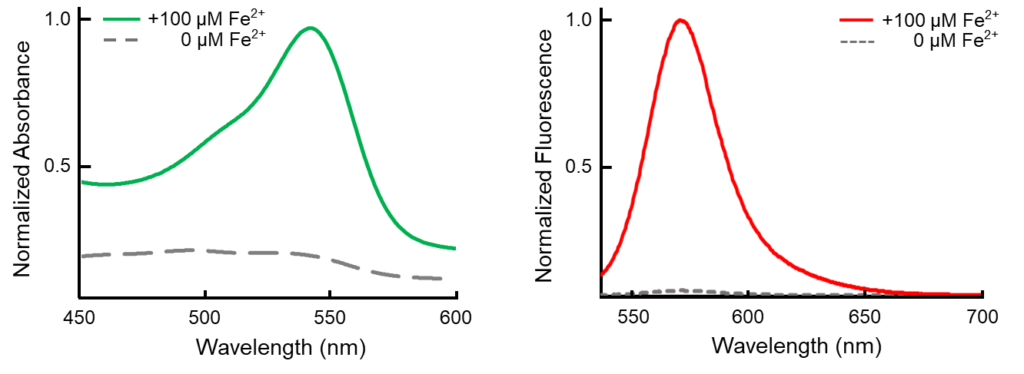
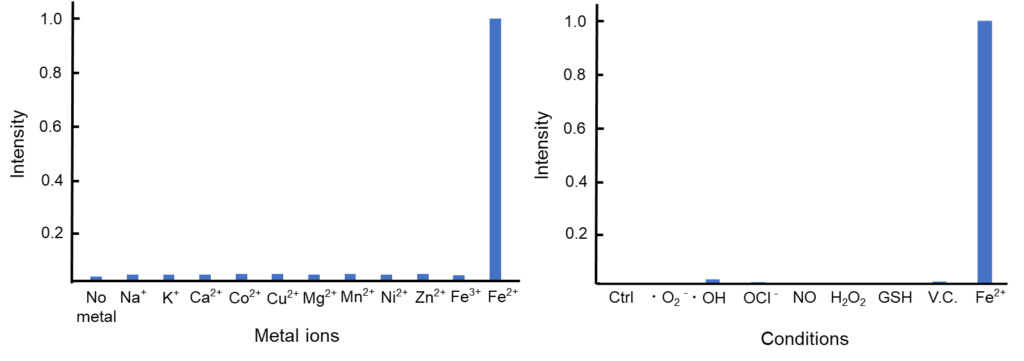
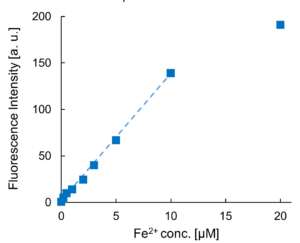
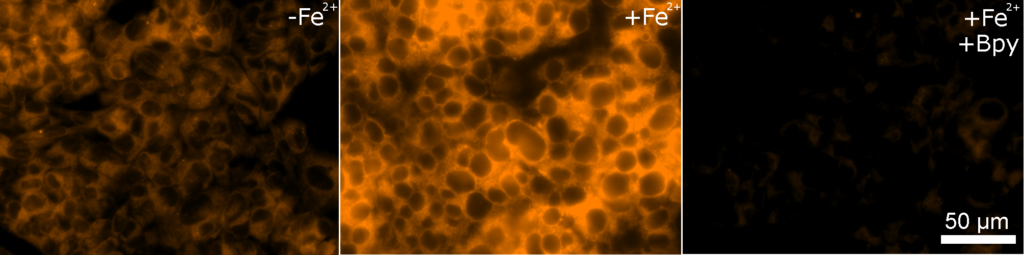
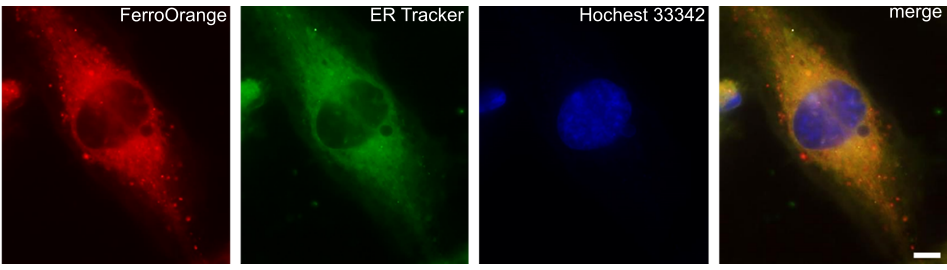
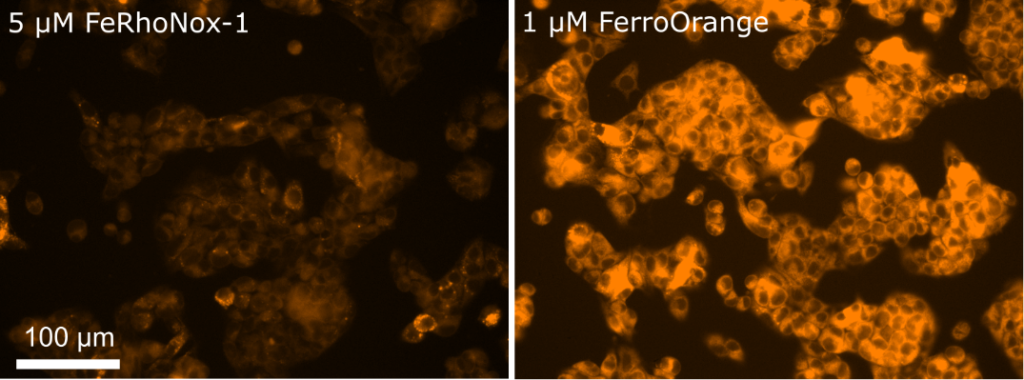
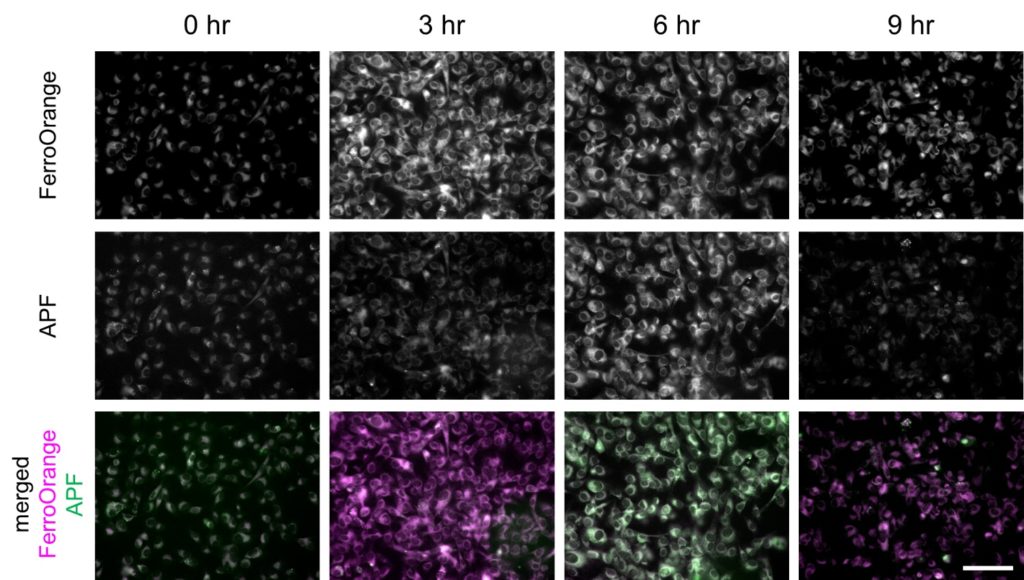
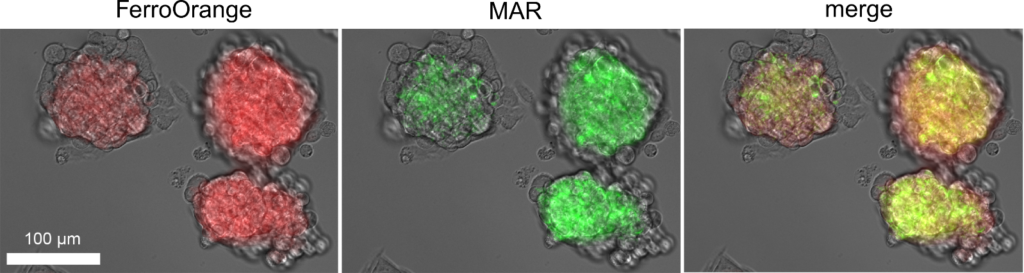
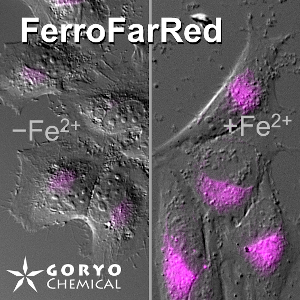
FerroOrange は RhoNox-4 としても知られる、遊離鉄 (II) イオン (Fe2+) のみを特異的に検出するオレンジ色蛍光プローブです。 鉄 (III) イオン (Fe3+) や鉄以外の 2 価の金属イオンでは蛍光強度は増加しません。またフェリチンなどにキレートされた鉄とも反応しません。FerroOrange は高い細胞膜透過性があり、迅速に反応した後は細胞内にとどまるため、ライブセルイメージングに使用できます。
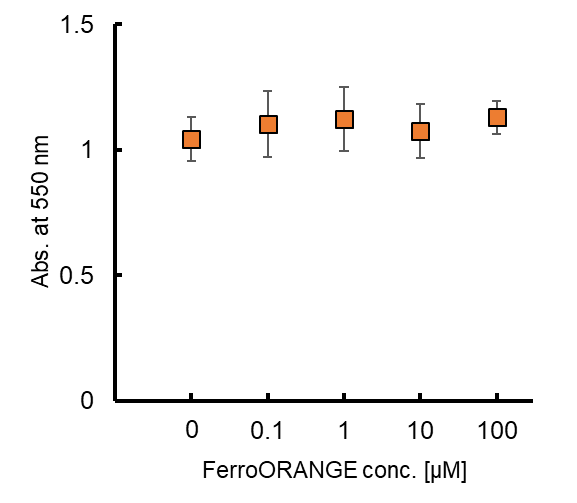
また、本試薬にキレート作用はございません。
FerroOrange は岐阜薬科大学 創薬化学大講座 薬化学研究室の永澤秀子先生、平山祐先生のご指導・ご協力のもと五稜化薬株式会社が製品化しました。
FerroOrange は Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT210-5×35nmol BioTracker FerroOrange Live Cell Dye
SCT210-35nmol BioTracker FerroOrange Live Cell Dye
の名前で販売されています。
![]()





 メールでのお問い合わせ
メールでのお問い合わせ
