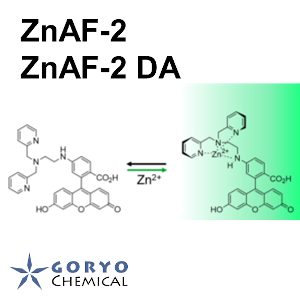
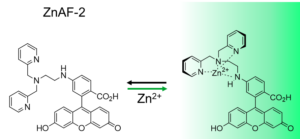
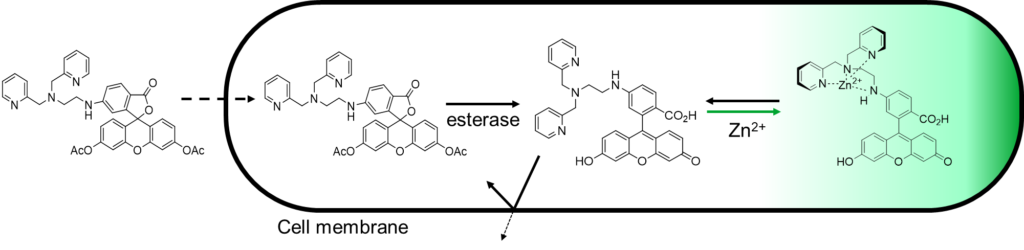
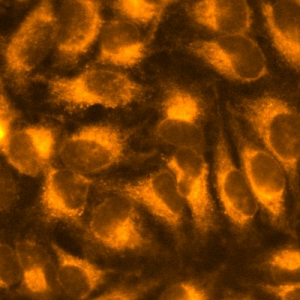
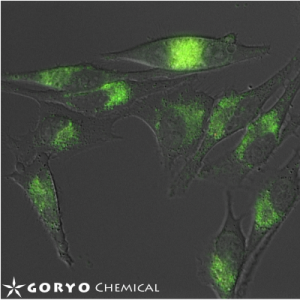
ZnAF-2, ZnAF-2 DA は亜鉛イオン (Zn2+) を検出するための蛍光プローブです。Zn2+ への高い特異性があり、カルシウム、マグネシウム、カリウム、ナトリウム、鉄など細胞中に多く存在する他のイオンとはほとんど反応しません。ZnAF-2 は細胞膜透過性がなく試験管や細胞外での Zn2+ の特異的な検出・定量に使われます。ZnAF-2 DA はジアセチル化された膜透過性のある試薬です。細胞内でアセチル基が分解され、細胞内に留まるため、細胞内 Zn2+ の時間変化の検出など、ライブイメージングに使用されます。
ZnAF は第一化学株式会社の登録商標です。この商標権は積水メディカル株式会社を経て五稜化薬株式会社に継承されています。
ZnAF-2, ZnAF-2 DA は Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT 031 BioTracker™ 515 Green Zn2+ Dye
SCT 032 BioTracker™ 515 Green Zn2+ DA Dye の名前で販売されています。
![]()





 メールでのお問い合わせ
メールでのお問い合わせ
