FeRhoNox-1は、遊離鉄 (II) イオン(Fe2+)を検出可能なゴルジ局在性の生細胞イメージング用蛍光プローブです。他の金属イオンには反応しないため、細胞中の Fe2+ を特異的に検出することができます。
また、本試薬にキレート作用はございません。
FeRhoNox-1 は Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT 030 BioTracker™ 575 Red Fe2+ Dye の名前で販売されています。
![]()
MetalloFluor™ Series
[遊離鉄 (II) イオン検出用蛍光プローブ]
570-590 nm:橙色
FeRhoNox-1は、遊離鉄 (II) イオン(Fe2+)を検出可能なゴルジ局在性の生細胞イメージング用蛍光プローブです。他の金属イオンには反応しないため、細胞中の Fe2+ を特異的に検出することができます。
また、本試薬にキレート作用はございません。
FeRhoNox-1 は Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT 030 BioTracker™ 575 Red Fe2+ Dye の名前で販売されています。
![]()
FeRhoNox™-1
製品情報
印刷する
| 名称 | 検出対象 | 膜透過性 | 反応 | Absmax(nm) | FLmax (nm) |
| FeRhoNox-1 | 遊離鉄 (Fe2+) | あり | 不可逆 | 540 | 575 |
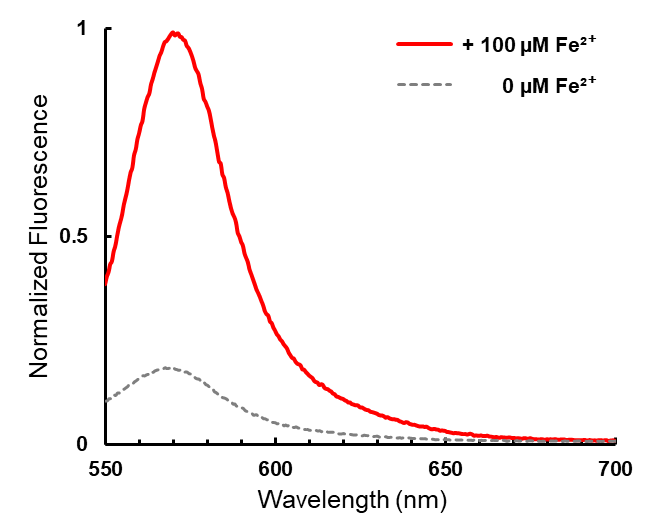
図1. Fe2+反応前後のFeRhoNox-1の蛍光スペクトル
FeRhoNox-1とFe2+を37℃、1時間反応させた。Fe2+を反応させると、575 nmをピークに蛍光強度上昇を示した。
HepG2 細胞に対して Fe(NH4)2(SO4)2 (FAS; 100 μM) を加えて、30 min インキュベートした後、5 μM のFeRhoNox-1を加えてさらにインキュベート。1 h 後、蛍光顕微鏡観察。
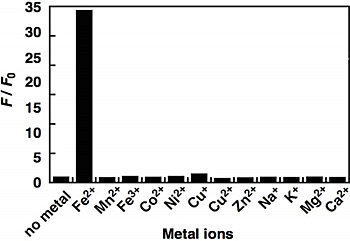
図2.FeRhoNox-1の 金属イオン選択性。
鉄(II)イオンのみに選択的に反応している。
FeRhoNox™-1
FeRhoNox-1 細胞イメージング例
印刷する
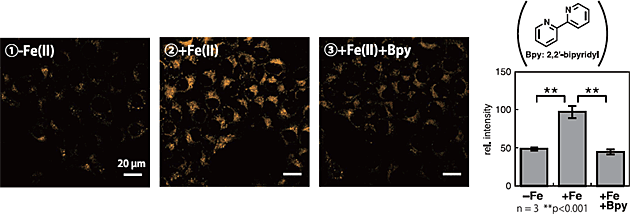
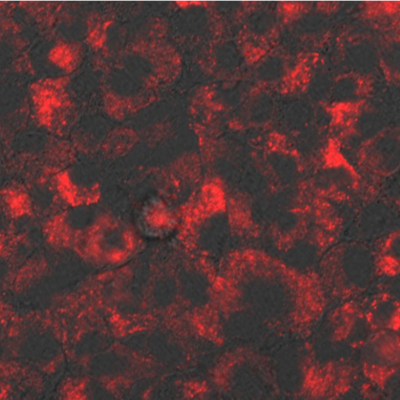
FeRhoNox-1 を用いた HepG2 細胞でのライブセルイメージング。(1) -Fe(II): 鉄イオン(100μM ferrous ammonium sulfate)を加えていない細胞。 (2) +Fe(II):鉄イオンを培地に添加 (3) +Fe(II)+Bpy:更に鉄 (II) イオンキレーターである Bpy を添加した場合。
(2) の Fe(II) で FeRhoNox-1 の蛍光増加が見られるが、(3) で蛍光強度が減少していることから、選択的に鉄 (II) イオンを検出していることがわかる。
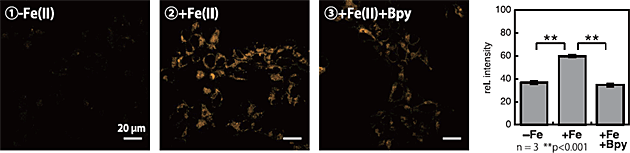
FeRhoNox-1 を用いた HEK293 細胞でのライブセルイメージング。(1)-Fe(II): 鉄イオンを加えていない場合、(2) +Fe(II): 鉄イオンを加えた場合、(3) +Fe(II)+Bpy: 更に Bpy を添加した場合。
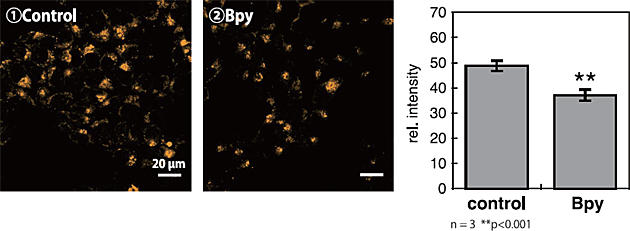
細胞内内在性鉄(II)イオンの検出。(2) Bpy添加によりシグナルが減少していることからFeRhoNox-1 により内在性鉄(II)が検出されていることがわかる。
*Bpy: 2,20-bipyridyl (Bpy)は細胞膜透過性の鉄(II)イオン選択的キレーターです。
パラフィン切片での使用は基本的にはできないとお考えください。
組織切片の鉄イオン検出には、凍結切片を軽くホルマリンで固定する方法が報告されています。以下の論文をご参照ください。
Mukaide et al., (2014) Histological detection of catalytic ferrous iron with the selective turn-on fluorescent probe RhoNox-1 in a Fenton reaction-based rat renal carcinogenesis model
Free Radical Research 48:990-995
http://dx.doi.org/10.3109/10715762.2014.898844
FeRhoNox-1 の溶媒として dimethyl sulfoxide (DMSO) を推奨しています。DMSO は infinity pure, ultra-pure などと表示されているできるだけ純度の高いものを準備し、開封後すぐにご使用ください。すぐに使用しない場合は、吸湿しないように分注して超低温フリーザーで保管しておくことをお勧めします。
理由として、DMSO は劣化すると硫化メチルなどの分解物が生成しますが、この分解物によって FeRhoNox-1 の蛍光バックグラウンドが上昇することがあるためです。
プローブは ER や Golgi に局在することが知られていますが、このプローブが検出する Fe2+ は細胞質の Fe2+ も反映しているのではないかと考えられています。ただし、これをきちんと検証した報告はありません
検出感度が最も高いのは FerroOrange です。赤色レーザーを使用したフローサイトメトリーには FerroFarRed が最適です。
FeRhoNox-1 は論文実績が豊富にあるため、既存の報告を確実に再現させたい場合に最適です。
| 型番 | 製品名 | Exmax (nm) | Emmax (nm) | 蛍光顕微鏡 | フローサイトメトリー (青色レーザー) |
フローサイトメトリー (赤色レーザー) |
プレートリーダー |
| AR2901-U5 | FeRhoNox-1 | 540 | 575 | 〇 | △ | - | 〇 |
| GC903 | FerroFarRed | 646 | 662 | 〇 | - | 〇 | 〇 |
| GC904 | FerroOrange | 542 | 572 | 〇 | △ | - | 〇 |
FeRhoNox-1, FerroOrange をレーザー励起で検出するためには、532 nm 等のグリーンレーザーの使用を推奨します。
蛍光色素一般に関する Q&A も参照してください