HySOxはHOCl (次亜塩素酸) を特異的に検出する蛍光試薬で、生細胞のイメージングに最適です。HySOxは中性水溶液中でほとんど蛍光を発しませんが、次亜塩素酸と反応すると、強蛍光化合物に変化し (励起波長 553 nm、蛍光波長 574 nm) 、蛍光強度の増大が観測されます。
HySOxは Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT 034 BioTracker™ 574 Red HOCL Dye の名前で販売されています。
![]()
ROSFluor™ Series
[次亜塩素酸 (HOCl) の特異的な検出に]
570-590 nm:橙色
HySOxはHOCl (次亜塩素酸) を特異的に検出する蛍光試薬で、生細胞のイメージングに最適です。HySOxは中性水溶液中でほとんど蛍光を発しませんが、次亜塩素酸と反応すると、強蛍光化合物に変化し (励起波長 553 nm、蛍光波長 574 nm) 、蛍光強度の増大が観測されます。
HySOxは Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT 034 BioTracker™ 574 Red HOCL Dye の名前で販売されています。
![]()
HySOx
製品情報
印刷する
| 製品名 | 検出対象 | 膜透過性 | 反応性 | Absmax (nm) | FLmax (nm) |
| HySOx | HClO | あり | 不可逆 | 553 | 574 |
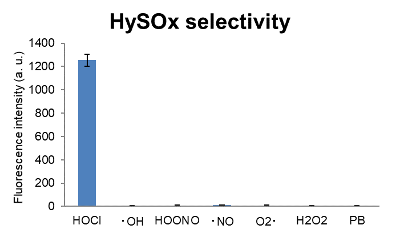
図1. 活性酸素種に対するHySOxの選択性
HySOxは次亜塩素酸とのみ反応しS/N比は約170倍を示した。
HySOx (最終濃度5 μM, コソルベントとして0.1 % DMF) を溶解したリン酸バッファー (0.1 M, pH 7.4) に、以下の活性酸素種生成系を添加 (最終濃度)。
励起波長553 nm、測定波長574 nm, slit width 2.5 nm, photon multiplier voltage 700V.
各活性酸素種生成条件
HOCl: NaOCl 5 μM
・OH: 過塩素酸鉄 (II) 50 μM, H2O2 100 μM
ONOO-: HOONO 5 μM
・NO: NOC18 5 μM
O2-・: KO2
H2O2: H2O2 100 μM
PB: リン酸バッファー (Negative control)
HySOx (最終濃度 5 μM, コソルベントとして0.1 % DMF) を溶解したリン酸バッファー (0.1 M, pH 7.4) に、終濃度 0-15 μMになるよう NaOCl を加え、スペクトルを測定した。また、定量性試験は NaOCl の終濃度 0-5 μMで行った。
励起波長 553 nm、測定波長 574 nm, slit width 2.5 nm, photon multiplier voltage 700 V.
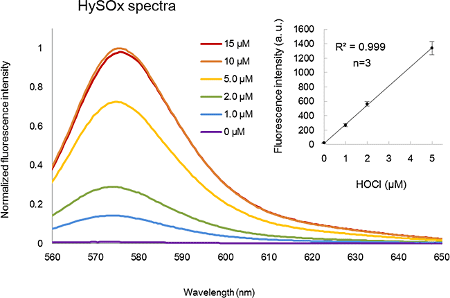
図2. HySOxの次亜塩素酸の濃度依存的なスペクトル変化
HySOx は次亜塩素酸とモル比 1:2 で飽和状態に達した。
(右上) 次亜塩素酸に対する HySOx の定量性
試験管内の反応において、HySOx は次亜塩素酸に対し濃度依存的な蛍光強度の増加を示した。
HySOx
U937 細胞のファゴサイトーシスにおける次亜塩素酸産生の観察
印刷する
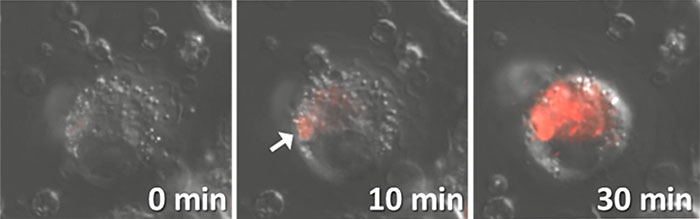
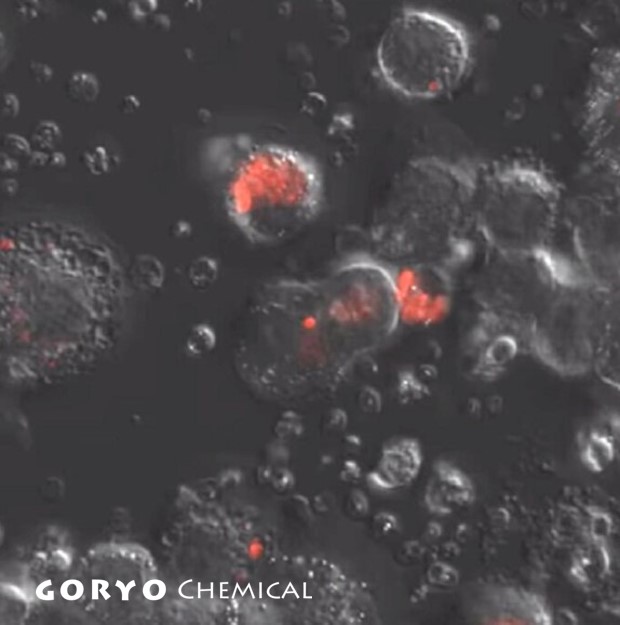
図1. ファゴサイトーシスに伴って次亜塩素酸を産生するU937 cell
PMA を加えて U937 cell の分化を誘導。
HySOx を DMF て溶解し、1 mM 溶液を作成。
1 mM 溶液をHBSSで希釈し、終濃度 5 μM の反応液を作成した。
培養容器から液体培地を除去し、HBSS で 2 回洗浄。
培養容器に反応液を加え、37℃で 30 分間培養。
培養容器から染色液を除去し、HBSS で 2 回洗浄。
新しいHBSSに置き換え、Zymosan A を加えて 37℃ で 30 分間タイムラプスイメージングを行った。
※ 使用顕微鏡: Leica DMI 6000 CS, 対物レンズ: 40倍
各製品のプロトコル推奨の溶媒を使用してください。多くの蛍光プローブは、最初に dimethyl sulfoxide (DMSO) または N,N-dimethylformamide (DMF) に溶解してからバッファー溶液などの水溶液で希釈します。水溶性が高くない物質は、ミリモルオーダーの水溶液を作るのが難しかったり、最初に有機溶媒に溶かしたほうが安定した水溶液を作成できるためです。
一級アミンと反応するNHS は水溶液中で分解やすいため、まずは脱水した DMSO に溶解してから、pH 8.4 前後の溶液に溶かしたタンパク質などとすみやかに混合しながら反応させてください。脱水 DMSO は試薬として販売されているほか、通常の DMSO に高温、減圧条件で乾燥させたモレキュラーシーブス 3A を添加して脱水することもできます。
有機溶媒は一般に長期間保存すると空気中の水分を吸ったり、酸化や紫外線の影響などで品質が低下します。品質が低下した溶媒を用いると、蛍光のバックグラウンドが上昇したり、反応性が低下することがあります。DMSO の場合はできるだけグレードの高いものを開封後すぐに分注して超低温フリーザーで保管すると比較的長く品質を保つことができるようです。この場合、吸湿させないために分注はなるだけ乾燥した環境で行い、また開封前に完全に室温に戻すようご注意ください。DMF についても湿気、高温、紫外線を避けて保管し、開封後はできるだけ早くご使用ください。
以下の表をご参照ください。
| 型番 | 製品名 | Exmax (nm) | Emmax (nm) | ・OH | ONOO— | HClO | H2O2 | O2-・ | 溶液中での ROS検出 |
培養細胞内でのROS検出 |
| GC3004-01 | OxiORANGE | 553 | 577 | + | - | + | - | - | + | + |
| GC3006-01 | HySOx | 553 | 574 | - | - | + | - | - | + | + |
| GC3007-01 | HYDROP | 492 | 518 | - | - | - | + | - | – | + |
| GC3008-01 | HYDROP-EX※ | 492 | 518 | - | - | - | + | - | + | – |
| SK3001-01 | HPF | 490 | 515 | + | + | - | - | - | + | + |
| SK3002-01 | APF | 490 | 515 | + | + | + | - | - | + | + |
| SK3003-01 | NiSPY-3 | 490 | 515 | - | + | - | - | - | + | + |
※HYDROP-EXは細胞膜透過性が低く、細胞外や溶液中の H2O2 の測定に適しています。一方 HYDROP はジアセチル化された試薬で、細胞外の H2O2 検出はできません。