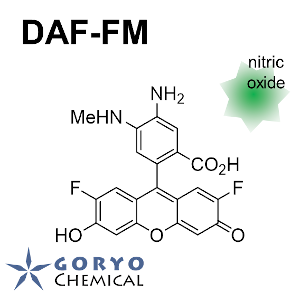
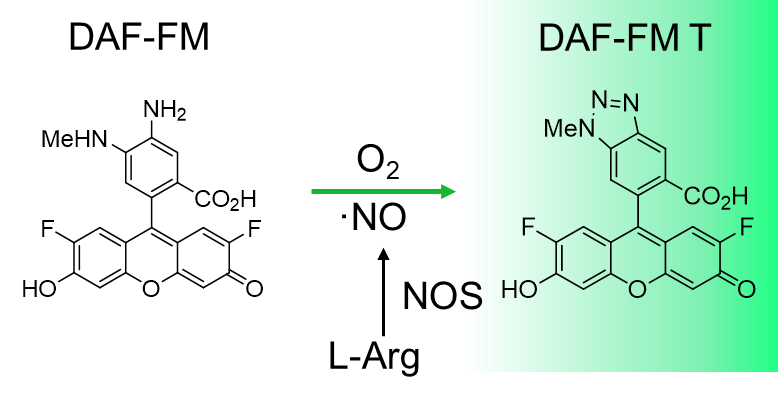
Diaminofluorescein-FM (DAF-FM) は一酸化窒素 (NO) を検出できる蛍光プローブです。そのままでほとんど蛍光を示しませんが、NO と反応すると強い緑の蛍光を発します。DAF-FM は DAF-2 を改良したもので、弱酸性領域でも安定した蛍光を示し、pH 6 以上で使用可能です。細胞膜透過性がなく、細胞外での NO 検出に適しています。
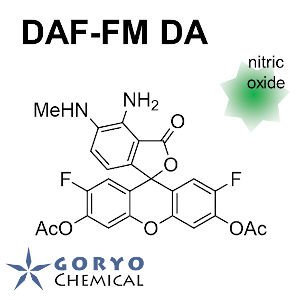
DAF-2 を用いた pH 7 付近のバッファー中での NO 検出限界は 5 nM と報告されています。 DAF-FM では蛍光強度は DAF-2 の 1.5 倍ありますので、若干高感度となると思われます。また DAF-2 DA や DAF-FM DA を用いて細胞内で検出する場合、細胞内の物質に妨害され感度がこれらより低下する可能性があります。








 メールでのお問い合わせ
メールでのお問い合わせ
