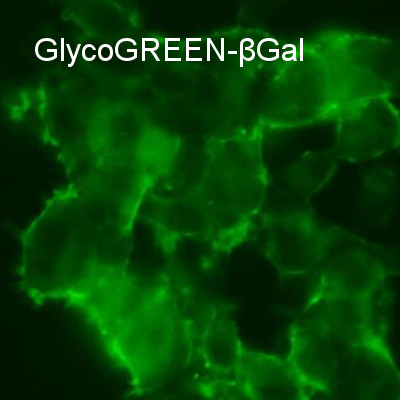
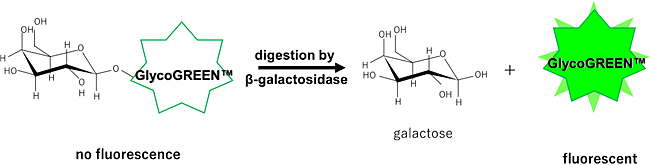
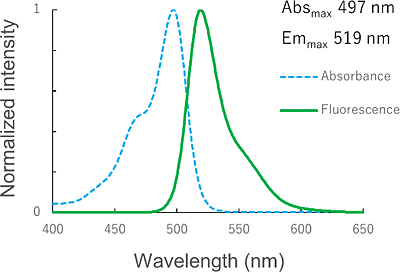
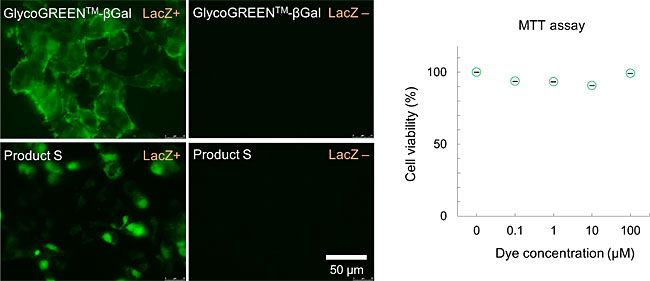
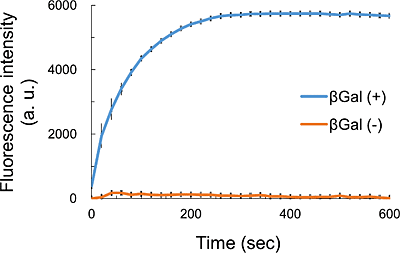
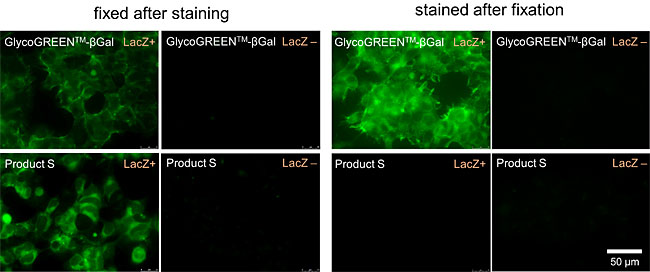
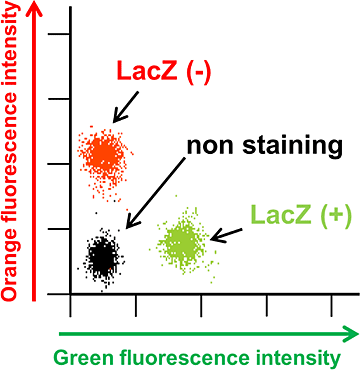
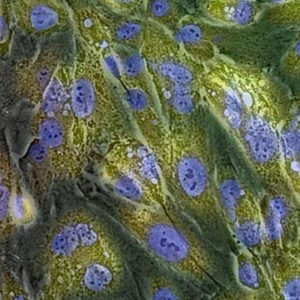
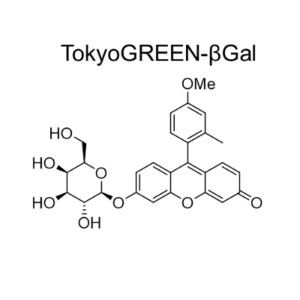
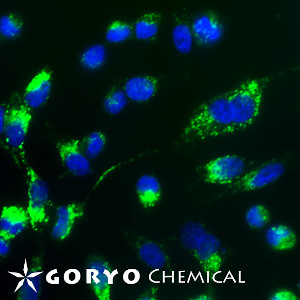
GlycoGREEN-βGal は β-ガラクトシダーゼ活性を蛍光で検出するための蛍光プローブです。最初は蛍光のない物質ですが、ガラクトシダーゼと反応して緑の蛍光物質を生成する蛍光基質です。膜透過性がありますが、反応後は細胞内の構造と弱く相互作用するため、細胞内に留まりやすくなります。また、毒性が極めて低いことから細胞機能への影響を最小限にしながら、生細胞のガラクトシダーゼ活性のイメージングに最適です。
遺伝子発現レポーターとしての lacZ の発現解析や、がん細胞マーカーとしての β-ガラクトシダーゼ活性の検出、また細胞老化によって上昇する β-ガラクトシダーゼ活性 (SA-β-gal) の検出などにご利用いただけます。
GlycoGREEN-βGal は Merck KGaA (Darmstadt, Germany) からも全世界にて
SCT025 BioTracker™ 519 Green β-Gal Dye の名前で販売されています。
![]()





 メールでのお問い合わせ
メールでのお問い合わせ
